קורס מושגי יסוד
5/5
₪130 המחיר המקורי היה: ₪130.₪49המחיר הנוכחי הוא: ₪49.
נלמד על החומרים המרכיבים את כל הדברים שבסיבינו, נמיין אותם, נלמד על התכונות הבולטות כגון מצבי צבירה, נקודת רתיחה והתכה, הולכה חשמלית ותכונות כימיות כגון תגובות שריפה. נלמד על החלקיקים שמרכיבים את החומר: אטומים ומולקולות ונלמד שפה חדשה שהיא שפת הכימאים: סימול היסודות , התרכובות ורישום תגובות כימיות.
מה נלמד בקורס?
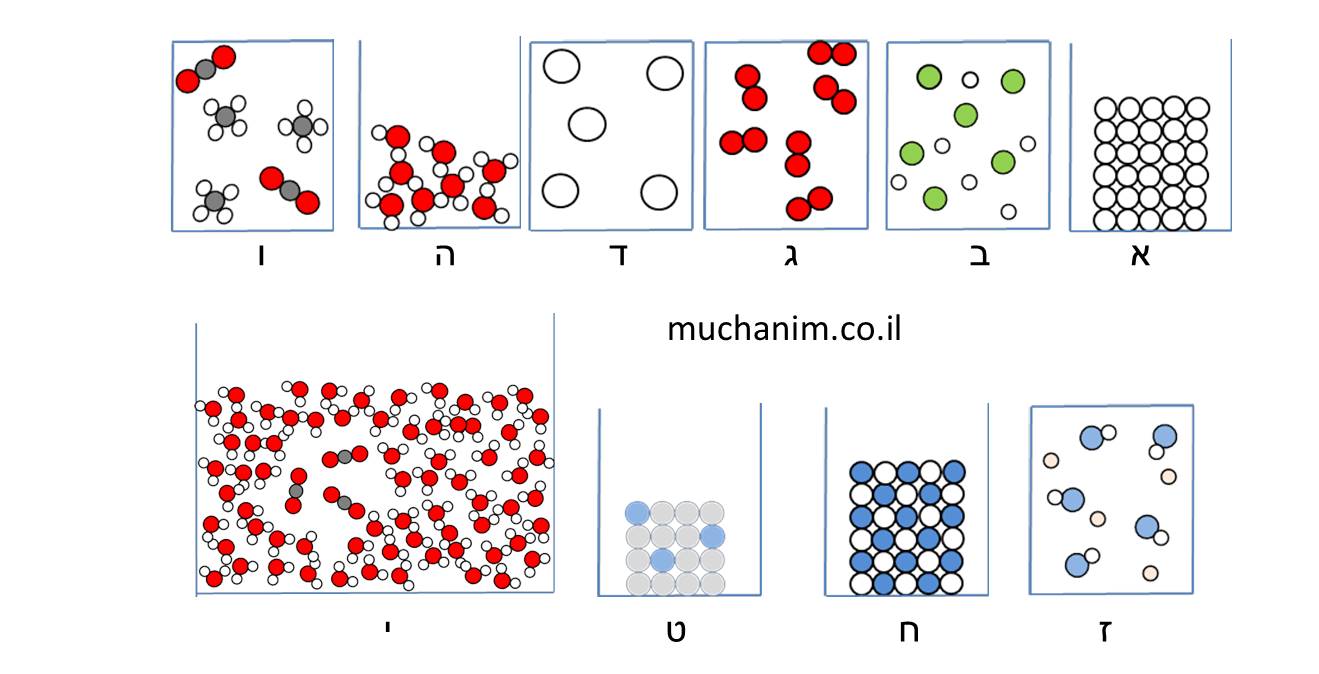
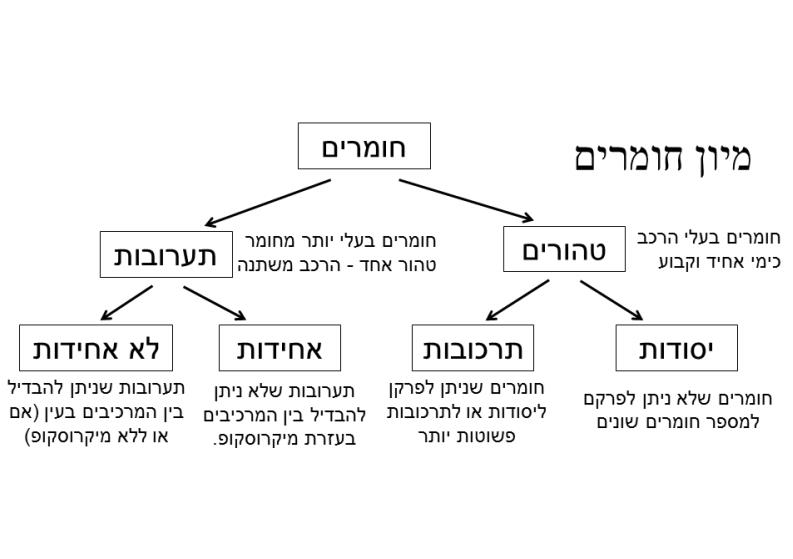
✔ נדע למיין חומרים ליסודות, תרכובות ותערובות
✔ נלמד על תכונות של חומרים:
מצבי צבירה
מעברים בין מצבי צבירה
נקודת רתיחה והתכה
הולכה חשמלית
מסיסות
תגובות כימיות
✔ נלמד על תורת החלקיקים:
אטומים
מולקולות
✔ נלמד את שפת הכימאים:
יסודות
תרכובות
תגובות כימיות
תכנית לימודים
₪130 המחיר המקורי היה: ₪130.₪49המחיר הנוכחי הוא: ₪49.
הקורס כולל
- כניסה לשנה
- 7 סרטוני וידיאו עם אנימציות 0.89 שעות צפיה
- 1 פתרונות מודרכים בוידיאו
- שאלות בגרות עם סרטוני פתרון מודרך
- 6 בחני הבנת הוידיאו
- סיכומים קצרים כולל איורים וטבלאות
- 6 תרגולים עם 27 שאלות כולל תשובות
- מבחן מסכם



חוות דעת
אין עדיין חוות דעת.